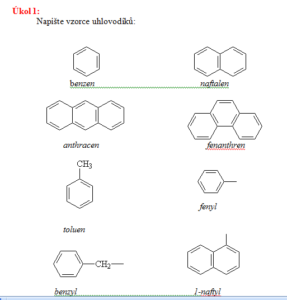
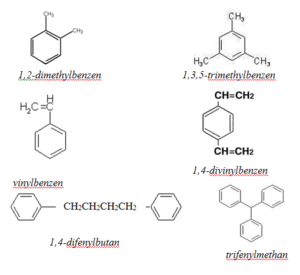
->
Charakteristika
- Aromatické uhlovodíky = areny
- Uhlovodíky obsahující minimálně jeden aromatický kruh (benzenové jádro)
- Měřením se zjistilo že π elektrony jsou delokalizovány = rovnoměrně rozloženy nad a pod rovinou kruhu
- Zaniká charakter jednoduchých a dvojných vazeb, vazby jsou rovnocenné
- Jsou velmi stálé – nepodléhají adičním reakcím jako alkeny a alkyny
- Podléhají hlavně substitučním reakcím (elektrofilní substituce)
Zdroje a příprava
- Vyskytují se v černouhelném dehtu
- Z ropy se získávají tzv. aromatizací (cyklizace, dehydrogenace)
Vlastnosti
- Benzen, toluen a xyleny jsou kapaliny
- Vícecyklické (naftalen, anthracen, fenanthren) jsou pevné látky
- Nerozpustné ve vodě, rozpustné v organických rozpouštědlech
- Pevné areny mají schopnost sublimovat
- Jedovaté, karcinogenní s typickým zápachem
- Jejich hořením vznikají saze
Rozdělení
- Monocyklické – jeden aromatický kruh
např. benzen, toluen, xylen, styren… - Polycyklické – kondenzovaná benzenová jádra
např. naftalen, anthracen, fenanthren - Nekondenzovaná (izolovaná) benzenová jádra
např. bifenyl, difenylmethan
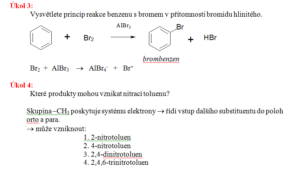
Reakce
- Při reakcích aromatických uhlovodíků se zachovává aromatický charakter
- Nejběžnější je elektrofilní substituce, kdy je jádro napadeno elektrofilním činidlem
- Elektrofilní činidlo se váže na π-elektrony aromatického jádra
Základní substituční reakce benzenu
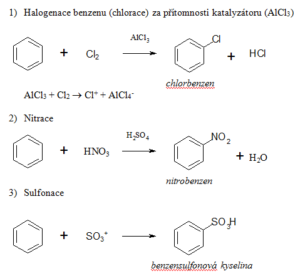
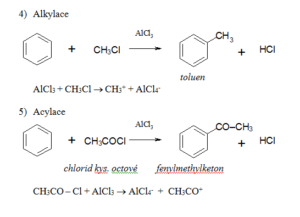
Disubstituovaný produkt
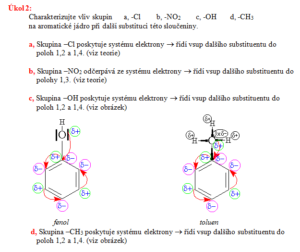
Indukční efekt
- Záporný indukční efekt –I
Je vyvolán atomem nebo skupinou atomů, které přitahují elektrony více než vodík ve vazbě C – H.
Přenáší se po σ elektronech.
např. –Cl, –OH, –NH2, –NO2 - Kladný indukční efekt +I
Je vyvolán atomem nebo skupinou atomů, které přitahují elektrony slaběji než vodík ve vazbě C – H.
Přenáší se po σ elektronech
např. –CH3
Mezomerní efekt
- Záporný mezomerní efekt –M
Vyvolávají jej atomy nebo skupiny atomů, které systému elektrony odčerpávají.
Přenáší se po π elektronech
Další substituent se může navázat do polohy 1,3 = meta
např. –NO2, –COOH, –CHO
Kladný mezomerní efekt +M
Vyvolávají jej atomy nebo skupiny atomů, které systému své elektrony poskytují.
Přenáší se po π elektronech
Další substituent se může navázat do polohy 1,2 = orto; 1,4 = para
např. halogeny, –NH2, –OH
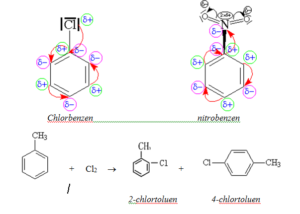
Adiční reakce benzenu
- Aromatické uhlovodíky se nechovají jako nenasycené uhlovodíky ® běžně nereagují adičními reakcemi.
- Ale účinkem tepla, katalyzátoru, ultrafialového záření může k těmto reakcím dojít.
- Převážně radikálové reakce
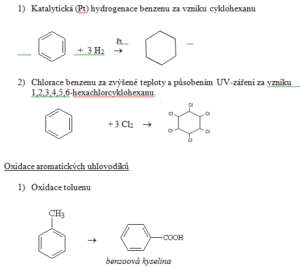
Zástupci
Benzen
- Bezbarvá, hořlavá, zdraví nebezpečná kapalina s charakteristickým zápachem.
- Narkotický jed, karcinogenní.
- Připravuje se izolováním z dehtu
- Používá se jako rozpouštědlo
- Výchozí látka pro přípravu dalších organických sloučenin (fenol, anilin, anhydridy, kyselina maleinová)
Toluen
- Kapalina podobná benzenu
- Používá se jako rozpouštědlo a pro výrobu organických látek (kyselina benzoová, umělé sladidlo sacharin)
- Výroba výbušnin TNT – 2,4,6-trinitrotoluen
- Konzervační a lehce narkotické účinky
- Používá se jako přípravek na srdce
- Zneužívána jako narkotická droga – předávkování způsobuje obrnu dýchacího centra a srdeční arytmie.
Styren (vinylbenzen)
- Základní monomer pro výrobu polystyrenu a butadienstyrenového kaučuku polymerací s but-1,3-dienem
Xyleny
- Slouží jako rozpouštědla
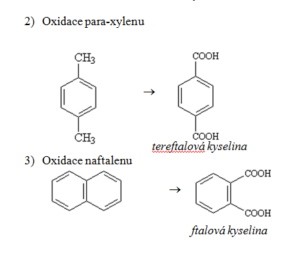
- P-xylen se používá k výrobě kyseliny tereftalové, umělá vlákna
- O-xylen se používá k výrobě anhydridu kyselinu ftalové
Naftalen
- Bílá krystalická sloučenina typického zápachu
- Snadno sublimuje
- Výroba kyseliny ftalové a barviv, dezinfekce, insekticid
Kumen
- Vzniká reakcí propylenu a benzenu
Používá se k výrobě fenolu a acetonu.